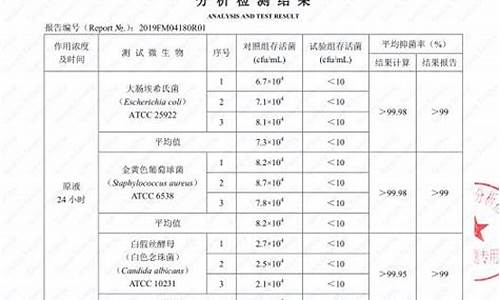
抑菌液成分检验报告单图片-抑菌液成分检验报告单
进口洗手液需要国妆备案
进口洗手液,属于非特殊类化妆品,要在国家药监局备案,如果有抑菌功效的是消毒产品,要做进口消字号产品备案。在卫计委备案。
扩展资料:
(一)、进口所需报关资料
1、进口非特殊用途备案申请表;
2、产品配方;
3、产品质量标准;
4、经卫生部认定的检验机构出具的检验报告及相关资料,按下列顺序排列:
A. 检验申请;
B. 检验受理通知书;
C.?产品说明书;
D. 卫生学(微生物、理化)检验报告;
E. 毒理学安全性检验报告;
5、产品原包装(含产品标签)。拟专为中国市场设计包装上市的,需同时提供产品设计包装(含产品标签);
6、产品在生产国(地区)或原产国(地区)允许生产销售的证明文件;
7、进口化妆品报关需提供其中文标签、货物入境检验检疫通关单、产品成分表、合同、发票、箱单和报检报关委托书等手续。
进口流程:
1、发货前客户提供产品标签设计稿、成分表、翻译进行评审产品;
2、签署合同(并提供相关公司证件及****备案)公司安排一对一客服跟进整个进口对接服务;
3、进口化妆品国家药监总局批文办理;
4、进口产品标签预审核及备案;
5、客户提前提供贸易合同、商业发票、装箱单、相关官方证书原件(原产地证书);
6、安排国外发货到大陆指定港口;
7、货到码头后进行迅速跟船公司换单,进行报检、报关;
8、海关出税单后缴税放行,安排运输送至客户仓库;
9、商检总局进行产品后续检验检疫,检验合格后出具检验检疫证书(CIQ证书),货物准予销售流通和使用。
资料来源:国家药监局—进口非特备案
消毒备案官网消毒备案
你好,微生物检测方法在中国药典2010年版二部附录XI J,具体方法为附录XI J微生物限度检查法
微生物限度检査法系检查非规定灭菌制剂及其原料、辅
料受微生物污染程度的方法。检查项目包括细菌数、霉菌数、
酵母菌数及控制菌检查。
微生物限度检查应在环境洁净度10 000级下的局部洁
净度100级的单向流空气区域内进行。检验全过程必须严格
遵守无菌操作,防止再污染,防止污染的措施不得影响供试品
中微生物的检出。单向流空气区域、工作台面及环境应定期
按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方
法》的现行国家标准进行洁净度验证。
供试品检查时,如果使用了表面活性剂、中和剂或灭活
剂,应证明其有效性及对微生物无毒性。
除另有规定外,本检査法中细菌及控制菌培养温度为
30?35°C;霉菌、酵母菌培养温度为23?28°C
检验结果以lg,lml、10g、10ml或10cm
2为单位报告,特
殊品种可以最小包装单位报告。
检验量
检验量即一次试验所用的供试品量(g、ml或cm
2
)。
除另有规定外,一般供试品的检验量为10g或10ml;膜剂
为100cm
2
贵重药品、微量包装药品的检验量可以酌减。要求检查沙门菌的供试品,其检验量应增加20g或20ml(其中
10g或10ml用于阳性对照试验)。
检验时,应从2个以上最小包装单位中抽取供试品,膜剂
还不得少于4片。
一般应随机抽取不少于检验用量(两个以上最小包装单
位)的3倍量供试品。
供试液的制备
根据供试品的理化特性与生物学特性,采取适宜的方法
制备供试液。供试液制备若需加温时,应均匀加热,且温度不
应超过451C。供试液从制备至加人检验用培养基,不得超过
1小时。
除另有规定外,常用的供试液制备方法如下。
1. 液体供试品
取供试品10ml ,加pH7.0无菌氯化钠-蛋白胨缓冲液至
100ml,混匀,作为1 : 10的供试液。油剂可加人适量的无菌
聚山梨酯80使供试品分散均匀。水溶性液体制剂也可用混
合的供试品原液作为供试液。
2. 固体、半固体或黏稠性供试品
取供试品10g ,加PH7.0无菌氯化钠-蛋白胨缓冲液至
100ml,用匀浆仪或其他适宜的方法,混匀,作为1 : 10的供试
液。必要时加适量的无菌聚山梨酯80,并置水浴中适当加温
使供试品分散均匀。
3. 需用特殊方法制备供试液的供试品
(1) 非水溶性供试品
方法1取供试品5g(或5ml),加至含溶化的(温度不超
过45'C)5g司盘80、3g单硬脂酸甘油酯、10g聚山梨酯80无
菌混合物的烧杯中,用无菌玻棒搅拌成团后,慢慢加人45"的
pH7. 0无菌氯化钠-蛋白胨缓冲液至100ml,边加边搅拌,使供
试品充分乳化,作为1 : 20的供试液。
方法2 取供试品10g,加至含20ml无菌十四烷酸异丙
酯(制法见附录H H无菌检査法中供试品的无菌检查项下)
和无菌玻璃珠的适宜容器中,必要时可增加十四烷酸异丙酯
的用量,充分振摇,使供试品溶解。然后加人45\:的pH7.0
无菌氯化钠-蛋白胨缓冲液100ml,振摇5?:L0分钟,萃取,静
置使油水明显分层,取其水层作为1 ? 10的供试液。
(2) 膜剂供试品.
取供试品100cm
2
,剪碎,加pH7.0无菌氯化钠-蛋白胨缓
冲液lOOmK必要时可增加稀释液),浸泡,振摇,作为1 : 10的
供试液(3) 肠溶及结肠溶制剂供试品
取供试品10g,加pH6. 8无菌磷酸盐缓冲液(用于肠溶制
剂)或pH7. 6无菌磷酸盐缓冲液(用于结肠溶制剂)至100ml,
置45t:水浴中,振摇,使溶解,作为1 :
10的供试液。
(4) 气雾剂、喷II剂供试品
取规定量供试品,置冰冻室冷冻约1小时,取出,迅速消
毒供试品开启部位,用无菌钢锥在该部位钻一小孔,放至室
温,并轻轻转动容器,使抛射剂缓缓全部释出。用无菌注射器
吸出全部药液,加至适量的PH7. 0无菌氯化钠-蛋白胨缓冲液
(若含非水溶性成分,加适量的无菌聚山梨酯80)中,混匀,取
相当于10g或10ml的供试品,再稀释成1 : 10的供试液。
(5) 贴剂供试品
取规定量供试品,去掉贴剂的保护层,放置在无菌玻璃或
塑料片上,粘贴面朝上。用适宜的无菌多孔材料(如无菌纱
布)覆盖贴剂的粘贴面以避免贴剂粘贴在一起。然后将其置
于适宜体积并含有表面活性剂(如聚山梨酯80或卵磷脂)的
稀释剂中,用力振荡至少30分钟,制成供试液。贴剂也可采
用其他适宜的方法制备成供试液。
(6) 具抑菌活性的供试品
当供试品有抑菌活性时,采用下列方法进行处理,以消除
供试液的抑菌活性,再依法检查。常用的方法如下。
① 培养基稀释法取规定量的供试液,至较大量的培养
基中,使单位体积内的供试品含量减少,至不含抑菌作用。测
定细菌、霉菌及酵母菌的菌数时,取同稀释级的供试液2ml,每
lml供试液可等量分注多个平皿,倾注琼脂培养基,混匀,凝固,
培养,计数。每lml供试液所注的平皿中生长的菌落数之和即
为lml的菌落数,计算每lml供试液的平均菌落数,按平皿法
计数规则报告菌数;控制菌检查时,可加大增菌培养基的用量。
② 离心沉淀法取一定量的供试液,500转/分钟离心3
分钟,取全部上清液混合。用于细菌检査。
③ 薄膜过滤法见细菌、霉菌及酵母菌计数项下的"薄
膜过滤法"。
④ 中和法凡含汞、砷或防腐剂等具有抑菌作用的供试
品,可用适宜的中和剂或灭活剂消除其抑菌成分。中和剂或
灭活剂可加在所用的稀释液或培养基中。
竹纤维成份报告
全国消毒产品网上备案官网?
消毒产品是没有全国性网上备案官网平台的,因为目前市场上存在的消毒产品都是地方卫生局批准的,查询其批准文件只能去当地卫生局。
全国消毒产品网上备案流程?
一、消字号需要在卫生厅进行备案,备案成功后可以在全国消毒产品网页链接上面进行查询,查询成功即为合法消字号产品。
二、备案流程:
1、确定产品性质属于抗抑菌产品或是消毒产品。
2、确定产品成分是否符合国标,切记不能添加西药和激素成分。
3、根据产品基本信息起草消字号产品资料(作为消字号检测依据)。
4、准备样品送检(消字号检测周期一般为3-4个月)。
5、备案安全评估报告。
6、网络备案。
第一类消毒产品:用于医疗器械的高水平消毒剂和消毒器械、灭菌剂和灭菌器械,皮肤/黏膜消毒剂,生物指示物、灭菌效果化学指示物;第二类消毒产品:除第一类产品外的消毒剂、消毒器械、化学指示物,以及带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂。消毒产品责任单位在第一类和第二类消毒产品首次上市前需要进行卫生安全评价。
消字号产品网上备案怎么回事?
一、消字号需要在卫生厅进行备案,备案成功后可以在全国消毒产品网页链接上面进行查询,查询成功即为合法消字号产品。
二、备案流程:
1、确定产品性质属于抗抑菌产品或是消毒产品。
2、确定产品成分是否符合国标,切记不能添加西药和激素成分。
3、根据产品基本信息起草消字号产品资料(作为消字号检测依据)。
4、准备样品送检(消字号检测周期一般为3-4个月)。
5、备案安全评估报告。
6、网络备案。
第一类消毒产品:用于医疗器械的高水平消毒剂和消毒器械、灭菌剂和灭菌器械,皮肤/黏膜消毒剂,生物指示物、灭菌效果化学指示物;第二类消毒产品:除第一类产品外的消毒剂、消毒器械、化学指示物,以及带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂。消毒产品责任单位在第一类和第二类消毒产品首次上市前需要进行卫生安全评价。
全国消毒产品网上备案查询官网?
一我们打开“全国消毒产品网上备案信息服务平台”(网址:)
二选择消毒产品责任单位查询,然后在下方的搜索框输入:山东华实药业有限公司(注:山东华实药业有限公司是秀霸二氧化氯消毒剂的生产厂家),点击“搜索”按钮。
三点击蓝色字体“山东华实药业有限公司”
四即可查看山东华实药业的所有平台备案产品,我们点击秀霸牌二氧化氯消毒粉II型这个链接,查看下该产品的备案信息。
五我们可以看到该产品的标签、检验报告、消毒产品卫生许可证等各项资质都非常齐全,是可以值得信赖购买的一款产品。
次氯酸怎么看编号?
1.
查看技术专利号和检验报告编号以及消毒产品备案信息首先,微酸性的定义是pH值范围6.20~6.80之间,pH>7不是次氯酸,pH6.20不属于微酸性,而是酸性;只公布专利没有明确专利号,难以确认专利真实性。检验报告编号以及产品备案信息不明确的是非正规消毒产品;洁控出品的威护星牌次氯酸消毒液,在优先确保安全的基础上,以杀菌与消臭为目的研发而成,具有稳定pH值的微酸性次氯酸水生成工艺。
2.
查看产品pH值是否有明确标识洁控微酸性次氯酸水生成设备运行过程中pH值允许范围精准智能控制在5.0~7.0之间,超出范围自动停止,生成过程中任何数值的波动范围控
微生物限度检查法
竹纤维是通过高科技手段从竹子中提取出来的一种绿色环保型纤维,它具有良好的透气性、瞬间吸水性、较强的耐磨性、良好的染色等优良特性。同时,竹纤维具有天然抗菌、抑菌、防螨、防臭和抗紫外线的作用。
药品领域的微生物检测及标准
再拿出来使用的话,如果时间不长,比如一周或半个月,可以直接使用,如果时间长了,建议活化后再用。
先活化转第二代后再使用。
培养方式,都可以,直立或者平放。
等到菌都长好了,就可以放到冰箱里,一般细菌长的都比较快,24小时就差不多了。
Str.pseudoporcinus是什么细菌
中国药典微生物限度检查法,为《中国药典》附录收载的关于药品微生物检查的法定方法。药品的不同剂型的微生物检测标准不同,具体如下:
1、制剂通则品种
制剂通则、品种项下要求无菌的制剂及标示无菌的制剂应符合无菌检查法规定。
2、口服给药制剂
细菌数每1g不得过l000cfu。每lml不得过100cfu。
霉菌和酵母菌数每lg或lml不得过100cfu。
大肠埃希菌每1g或lml不得检出。
3、耳、鼻及呼吸道吸入给药制剂
细菌数每1g、lml或l0cm?,不得过100cfu。
霉菌和酵母菌数每1g、lml或l0cm?,不得过10cfu。
金**葡萄球菌、铜绿假单胞菌每1g、lml或l0cm?不得检出。
大肠埃希菌鼻及呼吸道给药的制剂,每1g、lml或l0cm?,不得检出。
4、阴道、尿道给药制剂
细菌数每1g、lml或l0cm?,不得过100cfu。
霉菌数和酵母菌数每1g、lml或l0cm?应小于10cfu。
金**葡萄球菌、铜绿假单胞菌、白色念珠菌每1g、lml或l0cm?,不得检出。
5、直肠给药制剂
细菌数每1g不得过l000cfu。每lml不得过100cfu。
霉菌和酵母菌数每1g或lml不得过100cfu。
金**葡萄球菌、铜绿假单胞菌每lg或lml不得检出。
6、其他局部给药制剂
细菌数每1g、lml或l0cm?不得过100cfu。
霉菌和酵母菌数每1g、lml或l0cm?不得过100cfu。
金**葡萄球菌、铜绿假单胞菌每1g、lml或l0cm?不得检出。
7、含动物组织
含动物组织(包括提取物)的口服给药制剂每10g或10ml还不得检出沙门菌。
8、兼用途径制剂
应符合各给药途径的标准。
扩展资料
微生物限度检查法的注意事项:
1、当建立产品的微生物限度检查法时,应进行控制菌检查方法的验证,以确认所采用的方法适合于该产品的控制菌检查。若产品的组分或原检验条件发生改变可能影响检验结果时,检查方法应重新验证。
2、检查项目应当包括细菌数、霉菌数、酵母菌数及控制菌检查。
3、微生物限度检查应在环境洁净度10000 级下的局部洁净度100 级的单向流空气区域内进行。
4、检验全过程必须严格遵守无菌操作,防止再污染。单向流空气区域、工作台面及环境应定期按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行洁净度验证。
5、除另有规定外,本检查法中细菌及控制菌培养温度为30℃~35℃;霉菌、酵母菌培养温度为23℃~28℃。
6、检验结果以1g、1ml、10g、10ml、10c㎡ 为单位报告,特殊品种可以最小包装单位报告。
百度百科-中国药典微生物限度检查法
Str.pseudoporcinus是肺炎链球菌细菌。
肺炎链球菌于1881年首次由巴斯德(Louis Pasteur)及G. M. Sternberg分别在法国及美国从患者痰液中分离出。为革兰染色阳性,菌体似矛头状,成双或成短链状排列的双球菌,有毒株菌体外有化学成分为多糖的荚膜。
5%~10%正常人上呼吸道中携带此菌,有毒株是引起人类疾病的重要病原菌。
扩展资料
细菌和病毒属于微生物,只能在显微镜下看到。但它们是非常不同的东西,病毒是由蛋白质和核酸组成的一组小而不完整的细胞结构。必须寄生在活细胞中并复制,细菌和病毒属于微生物。
细菌体积大,一般光学显微镜都能看到,其生长条件不高。病毒相对较小,通常可以用放大一万倍以上的电子显微镜看到。病毒没有自己的生长和代谢系统,它们的生存取决于寄生在宿主(如人类)和依赖其他宿主的细胞中的代谢系统。
百度百科--细菌
百度百科--肺炎链球菌
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。
